فسیل
سَنگواره یا فُسیل (از زبان لاتین کلاسیک : Fossilis، یا زبان فرانسوی : Fossile، به معنای «به دستآمده از حفاری») به بازماندههای جانوران و گیاهان یا بازماندهها و آثار دیگر مثلاً ردپا گفته میشود. مثالهایی از بقایای جانداران عبارت اند از استخوان، صدف ، اسکلت خارجی ، مو ، روغن ، زغال سنگ ، دی ان ای یا حتی تصویر و ردی از جانداران یا باکتری ها که روی سنگها نقش بستهاند.
فرایند سنگوارهشدن فرآیندی نادر است زیرا بقایای طبیعی معمولاً تجزیه شده و دوباره وارد چرخۀ مواد میگردند. برای اینکه یک سازواره (جاندار)، سنگواره شود میبایست روی آن هرچه سریعتر با مواد رسوبی پوشیده شود. سنگوارهها و روند سنگوارگی انواع گوناگونی دارند. سنگوارهها معمولاً از خود مواد بازمانده از سازواره تشکیل شدهاند، ولی هستند سنگوارههایی که تنها شامل اثر و رد یک سازواره مثلاً رد پای یک دایناسور یا خزنده میشوند. به اینگونه سنگوارهها، سنگوارههای ردّی میگویند. دانش بررسی سنگوارهها دیرین شناسی نام دارد.
یکی از مناسبترین مکانها برای تشکیل سنگوارهها میتوان به حاشیهٔ دلتا ها و پیرامون کوههای آتشفشانی قدیمی که خاکستر از آنها متصاعد میشود و دریاهای کم عمق و یخچالها و باتلاقها نام برد. بیشتر دانشمندان معتقدند که فسیلها در دریاهای قدیمی قرار داشتهاند و در بین مواد رسوبی قرار گرفتهاند و در اثر فشار و گرمای زیاد، به شکل کنونی درآمدهاند.
از آثار سنگوارهها برای اثبات نظریههای زمین ساخت ورقهای و تکامل تدریجی استفاده شدهاست. در علم زمینشناسی مطالعهٔ دانشگاهی فسیلها در دو مبحث گیاهی و جانوری است که هر کدام به دوبخش بزرگسنگوارهها ماکرو فسیل و ریزسنگوارهها میکرو فسیل -و زیرشاخهٔ نانو فسیل ها - تقسیم شده و بر این اساس مطالعه میشوند. فسیل یا سنگواره را میتوان از مهمترین منابع اطلاعات دربارهٔ گذشتهٔ موجودات دانست. دانشمندان معتقدند نباید تمام فسیلهای یک منطقه را جمعآوری کرد. جمعآوری کامل نمونههای تریلوبیت ایران یکی از ناخوشایندترین اتفاقات مطالعاتی این حوزه است. مراغه که به بهشت فسیلی ایران معروف است نمونههای فسیلی خشکی را در خود جای داده که در کمتر جایی از دنیا این نمونههای حیوانات خشکی باقی ماندهاست.
فسیل برگ درخت راش اروپایی مربوط به ۲٬۵۸۸٬۰۰۰ تا ۳٬۰۰۰٬۰۰۰ سال پیش در موزهٔ تولو

فسیل یا سنگوارهٔ ماهیخزنده باراکوداسائورویدس که در دورهٔ تریاس میانه زندگی میکردهاست.
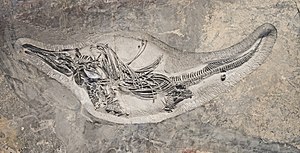
سنگوارهٔ یک ماهی